Transpoziție Bamberger
Transpoziția Bamberger este o reacție de transpoziție specifică fenil-hidroxilaminelor. Se realizează în mediu puternic acid și are loc transpoziția compușilor la 4-aminofenoli.[1][2][3] Reacția a fost denumită după chimistul german Eugen Bamberger (1857–1932).
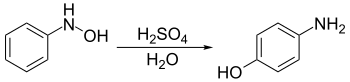
Hidroxilaminele de la care se pornește sunt de obicei sintetizate prin reacții de hidrogenare a nitrobenzenilor corespunzători, utilizând catalizatori de rodiu[4] sau zinc.[5]
Mecanism de reacție
modificareMecanismul transpoziției Bamberger începe cu protonarea N-fenil-hidroxilaminei notate cu 1. Poate avea loc de asemenea și o N-protonare, notată cu 2, care este favorizată, dar conduce la un produs nefavorabil. În urma reacției de protonare notată cu 3 se obține un intermediar cu ion nitreniu 4, care poate suferi atacul nucleofil al unei molecule de apă, în urma căruia se obține 4-aminofenolul 5, care este produsul final dorit al reacției de transpoziție.[6][7]
Vezi și
modificareNote
modificare- ^ Bamberger, E. (). „Ueber die Reduction der Nitroverbindungen”. Chemische Berichte. 27 (2): 1347–1350. doi:10.1002/cber.18940270229.
- ^ Bamberger, E. (). „Ueber das Phenylhydroxylamin”. Chemische Berichte. 27 (2): 1548–1557. doi:10.1002/cber.18940270276.
- ^ Harman, R. E. (), „Chloro-p-benzoquinone” (PDF), Org. Synth., 35: 22; Collective Volume, 4, p. 148
- ^ Oxley, P. W.; Adger, B. M.; Sasse, M. J.; Forth1, M. A. (). „N-ACETYL-N-PHENYLHYDROXYLAMINE VIA CATALYTIC TRANSFER HYDROGENATION OF NITROBENZENE USING HYDRAZINE AND RHODIUM ON CARBON”. Organic Syntheses. 67: 187. doi:10.15227/orgsyn.067.0187.
- ^ Kamm, O. (), „β-Phenylhydroxylamine”, Org. Synth., 4: 57; Collective Volume, 1, p. 445 (download PDF)
- ^ Sone, T.; Hamamoto, K.; Seiji, Y.; Shinkai, S.; Manabe, O. (). „Kinetics and Mechanisms of the Bamberger Rearrangement. Part 4. Rearrangement of Sterically Hindered Phenylhydroxylamines to 4-Aminophenols in Aqueous Sulphuric Acid Solution”. Journal of the Chemical Society, Perkin Transactions 2. 1981 (2): 1596–1598. doi:10.1039/P29810000298.
- ^ Kohnstam, G.; Petch, W. A.; Williams, D. L. H. (). „Kinetic Substituent and Isotope Effects in the Acid-Catalysed Rearrangement of N-Phenylhydroxylamines. Are Nitrenium Ions Involved?”. Journal of the Chemical Society, Perkin Transactions 2. 1984 (3): 423–427. doi:10.1039/P29840000423.