2,2,4-trimetilpentan
| 2,2,4-trimetilpentan | |
 | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 540-84-1 |
| ChEMBL | CHEMBL1797261 |
| PubChem CID | 10907 |
| Formulă chimică | C₈H₁₈[1] |
| Masă molară | 114,141 u.a.m.[2] |
| Proprietăți | |
| Densitate | 0,688 g/cm³ |
| Punct de topire | −107,38 °C |
| Punct de fierbere | 99,3 °C |
| Indice de refracție(nD) | 1,39145 |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
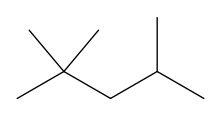
2,2,4-trimetilpentanul, cunoscut și ca izooctan sau izo-octan, este un compus organic cu formula (CH3)3CCH2CH(CH3)2. Este unul dintre numeroșii izomeri ai octanului (C8H18). Acest izomer în particular este special deoarece este standardul cu valoarea 100 pentru cifra octanică (punctul zero este n-heptan). Este o componentă importantă a benzinei, folosită frecvent în proporții relativ mari pentru a crește rezistența la detonare a combustibilului (agent antidetonant). [3]
Conform terminologiei substanțelor organice, denumirea de izooctan ar trebui să fie rezervată izomerului 2-metilheptan. Cu toate acestea, 2,2,4-trimetilpentanul este de departe cel mai important izomer al octanului și din punct de vedere istoric i s-a atribuit acest nume. [4]
Obținere
modificareIzooctanul este produs pe scară largă în industria petrolului prin alchilarea izobutenei cu izobutan. Acest proces se desfășoară în prezența catalizatorilor acizi.[5]
De asemenea, poate fi produs din izobutilenă printr-un proces de dimerizare, folosind catalizator Amberlyst (rășină schimbătoare de ioni) pentru a obține un amestec de izo-octene. Hidrogenarea acestui amestec produce 2,2,4-trimetilpentan. [6]
Vezi și
modificareNote
modificare- ^ a b „2,2,4-trimetilpentan”, 2,2,4-Trimethylpentane (în engleză), PubChem, accesat în
- ^ „2,2,4-trimetilpentan”, 2,2,4-Trimethylpentane (în engleză), PubChem, accesat în
- ^ Arno Reglitzky; Andrea Schütze; Klaus Reders (). „Automotive Fuels”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_719.pub2. ISBN 978-3527306732. Lipsește
|last1=în Authors list (ajutor) - ^ Clayden, Jonathan (). Organic chemistry (ed. Reprinted (with corrections).). Oxford [u.a.]: Oxford Univ. Press. pp. 315. ISBN 978-0-19-850346-0.
- ^ Joseph A. Kocal; Paul T. Barger; Robert J. Schmidt; James A. Johnson (). „Alkylation”. Kirk‐Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.0112112508011313.a01.pub2. ISBN 0471238961. Lipsește
|last1=în Authors list (ajutor) - ^ Dimerization of isobutylene, Amberlyst.com