Compuși halogenați
Compușii halogenați (denumiți și combinații halogenate și haloalcani sau haloizi alchil, pentru cei derivați de la alcani) [1] sunt o clasă de compuși organici care derivă formal de la hidrocarburi, prin înlocuirea atomilor de hidrogen cu atomi de halogen, respectiv: fluor, clor, brom sau iod.[2]:p. 418
Compușii sunt răspândiți și în natură; de exemplu, bromometanul este un component al apelor oceanice.[3]
Izomerie structurală
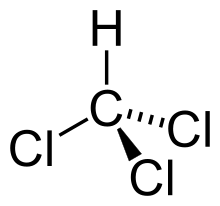
modificareNumărul compușilor izomeri structurali care pot lua naștere astfel este foarte mare. Numai de la metan derivă 4 compuși halogenați, care sunt CH3Cl, CH2Cl2, CHCl3 si CCl4. De la etan, un alt exemplu, sunt posibili și cunoscuți 9 derivați clorurați: CH3CH2Cl, CH3CHCl2, CH3CCl3, CH2ClCCl3, CHCl2CCl3, CCl3CCl3, CH2ClCH2Cl, CH2ClCHCl2, CHCl2CHCl2.[2]:p. 418
Teoria[care?] prevede existența a 29 derivați clorurați ai propanului, 666 ai n-hexanului, 1998 ai n-heptanului, și tot atâția derivați cu fiecare din ceilalți halogeni. Numai un mic număr dintre aceștia au fost preparați și au importanță practică.[2]:p. 418
Proprietăți fizice
modificareCompușii halogenați sunt substanțe incolore (cu excepția celor poliiodurați). Primii termeni din seria omoloagă a halogeno-alcanilor sunt gazoși la temperatura obișnuită, ceilalți sunt lichizi. Termenii inferiori ai seriei au puncte de topire scăzute, cei superiori și derivații aromatici disubstituiți (în poziție pară), la fel și cei polisubstituiți, sunt solizi.[2]:p. 427
Densitatea compușilor bromurați și iodurați este, în general, mai mare decât a apei, a celor monoclorurați ceva mai mică. Densitatea compușilor iodurați este mai mare decât cea a compușilor bromurați corespunzători, iar densitatea compușilor bromurați mai mare decât a compușilor clorurați (ρ(CH3I)=2,29; ρ(CH3Br)=1,73; ρ(CH3Cl)=0,953).[2]:p. 427
Compușii halogenați sunt practic insolubili în apă; în dizolvanții organici, cum sunt hidrocarburile, alcoolii, eterul, se dizolvă ușor. Compușii halogenați alifatici au miros dulceag și proprietăți narcotice. În concentrație mare sunt toxici. Clorura, dar mai ales bromura și iodura, de benzil sunt puternic lacrimogene.[2]:p. 427
Note
modificare- ^ Dicționar de chimie John Daintith, traducere de Mihaela Rudeanu și Lia Cojocaru; ediția a VI-a, Editura All, 2010, București; pag. 244, ISBN 978-973-684-725-7
- ^ a b c d e f Costin D. Nenițescu Chimie Organică, vol. I, ediția a VII-a, Editura Didactică și Pedagogică, 1973
- ^ Gordon W. Gribble (). „Naturally Occurring Organohalogen Compounds”. Acc. Chem. Res. 31 (3): 141–152. doi:10.1021/ar9701777.