Durere
| Acest articol are nevoie de atenția unui expert în medicină. Recrutați unul sau, dacă sunteți în măsură, ajutați chiar dumneavoastră la îmbunătățirea articolului! |
| Acest articol sau această secțiune nu este în formatul standard. Ștergeți eticheta la încheierea standardizării. |
Durerea este, conform I.A.S.P. (International Association for the Study of Pain) o senzație și o experiență senzitivă și emoțională neplăcută, asociată cu o leziune tisulară existentă sau potențială, sau descrisă ca o astfel de leziune. (Merskey, 1986) Această definiție implică atât factori senzitivi (de ex. nocicepția) cât și emoționali (ex. suferința). Se formulează de asemenea evenimente "actuale" dar și "potențiale".
| Durere | |
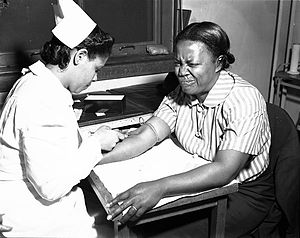 | |
| Specialitate | neurologie primary care[*] anesteziologie medicină de urgență Îngrijire paliativă |
|---|---|
| Clasificare și resurse externe | |
| ICD-9 | 338 |
| ICD-10 | R52.9 |
| ICD-11 | |
| DiseasesDB | 9503 |
| MedlinePlus | 002164 |
| MeSH ID | D010146[1] |
| Modifică date / text | |
Etimologie și termeni
modificareCuvântul "durere" derivă, în limba română din latinescul "dolor"; în terminologia utilizată în terapia durerii se mai folosesc termeni ce derivă din rădăcina indo-europeană "algo", care la greci (algeo) definea durerea fizică (nevralgie, hiperalgezie, analgezie), rădăcina "angh" (din greacă, latină și sanscrită - intră în constituția cuvintelor angină, anxietate) și rădăcina "spao" (din lb. greacă, spasm). Dacă pentru durere se mai folosește și sinonimul "algie", pentru suprimarea durerii, în limba română se folosește cuvântul "analgezie" (an-fără, algos-durere) și algeziologie pentru disciplina care studiază durerea și tratarea sa.
Fiziologie
modificareUzual durerea semnalează o leziune tisulară prezentă sau iminentă permițând prevenirea sau agravarea leziunii având un rol protector. Singurul stimul extern cauzator de leziune care nu este recunoscut decât foarte târziu prin durere este radiația. Transmiterea informațiilor nociceptoare poate fi modulată (creșterea sau scăderea pragului, sensibilizare) în cornul dorsal medular, dar și la alte nivele. Același stimul nociceptiv evocă în creier răspunsuri diferite după cum subiectul este în stare de alarmă, în stare de veghe, somnolent, în somn profund sau sub influența drogurilor/medicamentelor.
Nu există măsurători obiective pentru durere. Putem ști că o persoană “are durere“ doar pe baza afirmațiilor sau acțiunilor sale. Aceste acțiuni pot fi măsurate obiectiv, dar aceste măsurători nu pot să evalueze evenimentele care au dus la apariția lor. Impulsurile nociceptive pot fi, teoretic, măsurate dar nu pot defini gradul de suferință și nici răspunsul personal. Măsurarea răspunsului nu permite identificarea stimulului și stimulul nu poate fi măsurat. Durerea inițiază un răspuns complex neuro-umoral care inițial ajută menținerea homeostaziei în prezența unei injurii sau afecțiuni acute. Dacă aceste leziuni sunt excesive, durerea poate deveni cauzatoare de morbiditate. Răspunsul fiziologic al țesuturilor la injurie și durere acută este similar indiferent dacă are drept sursă actul chirurgical, trauma, arsura sau afectarea viscerală. Intensitatea depinde de extensia leziunii dar și de experiența fiecăruia. Transmisia durerii acute implică activarea receptorilor senzitivi pe fibrele periferice tip C: nociceptorii. Odată lezat țesutul sau inflamația realizată, acțiunea prostanoidelor, bradikininei (BK), serotoninei, ș.a. asupra receptorilor lor joacă un rol major în sensibilizarea și activarea fibrelor C. Leziunea țesuturilor produsă de injurie, boală sau inflamație eliberează substanțe endogene în fluidul extra-celular care înconjură nociceptorii. Aceste substanțe includ H+, K+, serotonina, histamina, prostaglandinele, bradikinina, substanța P (SP) și multe altele. Receptarea inițială a stimulilor dureroși este realizată de neuroni aferenți primari cunocuți ca nociceptori. Recepția stimulilor noxici se produce în terminațiile nervoase specializate funcțional din piele, mușchi, articulații, viscere și dura mater. Stimulii noxici cutanați (mecanici, termici, chimici) sunt transferați prin nociceptorii care răspund cel mai bine la stimuli mecanici (mecano nociceptori), mecanici și termici (mecano-termo nociceptori) sau mecanici, termici și chimici (nociceptori polimodali). Tipurile comune de nociceptori cutanați sunt mecano-receptorii Adelta și fibrele tip C. Terminații nociceptive mai sunt localizate în mușchi, fascia și adventicia vaselor sanguine, articulații, dura mater și viscere.
Clasificare durerii
modificare- Durerea acută: definită ca o durere de scurtă durată sau cu sursă care poate fi identificată. Durerea acută este mecanismul prin care organismul atenționează asupra afectării țesuturilor sau a unei boli. Este rapidă, tăioasă urmată de o durere acută. Este localizată la început într-o arie bine delimitată, după care difuzează. Acest tip de durere răspunde de obicei foarte bine la medicație.
- Durerea cronică este acel tip de durere cu durată mai mare de 6 luni, asociată de obicei cu un anumit tip de rănire sau de boală. Această durere este fie constantă, fie intermitentă și nu ajută organimsul pentru prevenirea afecțiunii. Medicația trebuie administrată de un personal de specialitate. Eventuala cinguloctemie - o neurointervenție care deconectează partea anterioară a girului cingului - poate fi utilizată în cazuri extreme pentru tratarea durerilor cronice. Post operație, pacienții vor primi în continuare impulsuri dureroase din corp, dar nu vor mai avea senzaṭia conṣtientă de durere.
- Durerea fiziologică poate fi grupată în funcție de sursa și de nociceptori ( neuroni care detectează durerea)
- Durerea cutanată, cauzată de rănirea țesuturilor superficiale ale pielii. Terminațiile nervoase ale nociceptorilor se termină aproape sub dermă, și datorită relativei mari concentrări de terminații nervoase produc o durere bine localizată, bine definită și de scurtă durată. Astfel dureri se întîlnesc la tăieri accidentale, la arsuri de grad 1 sau ulcerații.
- Durerea somatică își are originea în ligamente, tendoane, oase, vase sanguine. Este detectată prin intermediul nociceptorilor somatici. Datorită numărului mic de receptori din această zonă, durerea produsă este „surdă”, puțin localizată și de durată mai mare decît durerea cutanată; se întîlnește de obicei la luxații sau fracturi osoase.
- Durerea viscerală, durerea datorată organelor interne. Nociceptorii viscerali sunt localizați în interiorul organelor interne sau a cavităților. Lipsa mai pronunțată a nociceptorilor din această zonă determină ca durerea resimțită să fie mai intensă și cu o durată mai mare comparativ cu durerea somatică. Durerea viscerală este extrem de greu de localizat, iar eventualele răni ale diferitelor organe determină radierea durerii, adică localizarea în cu totul altă parte față de sursă. Ischemia cardiacă este un astfel de exemplu de durere viscerală. Senzația de durere este de obicei localizată la nivelul părții superioare a pieptului, cu localizare limitată, sau ca durere la nivelul umărului stîng, a brațului stîng, sau chiar a degetelor mîinii stîngi. Acest lucru se poate explica prin aceea că receptorii viscerali excită neuronii măduvei spinării care primesc semnale și de la țesuturile cutanate. Creierul asociază aceste excitări ale neuronilor respectivi ca datorîndu-se semnalelor transmise de piele sau de mușchi, transmiterea semnalelor de către receptorii viscerali este interpretată de creier ca provenind din piele. Această teorie conform căreia receptorii viscerali și somatici transmit semnalele în aceeași zonă a măduvei spinării este numită ipoteza Ruch
- Durerea membrului fantomă apare la persoanele care au suferit operația de amputare a unui membru, sau la persoanele care nu sesizează stimulii fizici. Se întîlnește la amputați sau paraplegici.
- "Neuropathic pain" sau neuralgia este durerea rezultată ca urmare a distrugerii neuronului sau afectării acestuia. Acest tip de durere duce la întreruperea abilității senzorilor nervoși de a transmite corect informația către talamus, iar de aici creierul este cel care interpretează stimulii dureroși, este evident că nu se ca cunoaște cauza durerii.
Baze anatomofiziologice
modificareDurerea apare datorită stimulării unor receptori specializați (nociceptori), și/sau fibrelor nervoase aferente. Nociceptorii pot fi clasificați astfel:
- mecanoreceptori - răspund la stimuli fizici.
- chemoreceptori pentru mediatorii chimici periferici ai durerii ( histamina, serotonina, bradikinina, PGE1). Două tipuri de nociceptori Aδ și fibrele C mediază durerea "rapidă" și "lentă". Fibrele Aδ sunt puțin mielinizate și transmit semnale cu o viteză între 6-30m/sec, ei fiind mediatorii pentru "durerea rapidă". Acest tip de durere este resimțit la 1/10 sec după stimulare, este descrisă ca fiind o durere înțepătoare, acută.
Durerea lentă, mediată de fibrele C (nemielinizate) transmit semnale nervoase cu o rată de 0,5-2 m/sec, fiind o durere pulsatorie, arzătoare și pulsatorie. Este cazul durerii provocate de substanțele chimice.
Transmisia durerii către sistemul nervos central
modificarePercepția durerii are loc atunci cînd nociceptorii sunt stimulați și transmit semnale către neuronii senzitivi din măduva spinării. Acești neuroni eliberează glutamat, un excitant major al neutrasmiterii de la un neuron la altul. Semnalul este transmis către talamus, acolo unde are loc percepția durerii. De aici, semnalul nervos ajunge la cortexul senzitiv, moment în care fiecare individ devine conștient de durere. Sunt 2 căi de trasmitere a durerii către SNC: calea neospinotalamică (durere rapidă) și calea paleospinotalamică (durere lentă)
- Durerea rapidă via fibrele Aδ se termină în lamina I (lamina marginalis) din coarnele dorsale a măduvei. A doua trasmitere are loc prin intermediul tractului neospinotalamic, se amplifică la nivelul fibrelor nervoase care traversează linia mediană prin comisura anterioară și se îndreaptă ascendent către partea anterolaterală. De aici o a treia transmisie are loc prin neuroni către cortexul somatosenzitiv. Durerea rapidă poate fi localizată ușor dacă fibrele Aδ sunt stimulate împreună cu receptorii tactili.
- Durerea lentă este transmisă via fibrele C către lamina II și III (substanța gelatinoasă), de aici neuronii transmițînd-o către lamina V, situată în cornul dorsal al măduvei spinării. De aici se intersectează cu fibrele durerii rapide, traversează în partea opusă via comisura anterioară, traversează ascendent pînă în calea anterolaterală. Acești neuroni se termină în creier aproximativ o zecime de fibre oprindu-se în talamus, iar restul în măduvă și mezencefal.
Căile aferente:
modificare- fibre senzitive nociceptive, somatice (fibre slab mielinizate), și vegetative (fibre nemielinizate C), incluse in nervii cranieni.
- căile ascendente ale sensibilității dureroase formează fasciculul spinotalamic lateral.
Centrii de integrare și percepere a durerii:
modificare- centrii talamici (percepere inconștientă, nelocalizată însoțită de alertă generală)
- sistemul limbic care coordonează componenta afectivă.
- centrii corticali aflați în lobii parietali.
Căile descendente de suprimare a durerii: cortexul orbitar, substanța cenușie periapeductală, bulbul inferior, cornul dorsal al măduvei spinării.
Din punct de vedere biochimic în farmacologia durerii sînt implicate foarte multe substanțe: serotonina, histamina, bradikinina (întilniți la nivelul nociceptorilor mediatori algogeni), endorfine, dinorfine, enkefaline, endomorfine, (neuromediatori peptidergici).
Farmacodinamie
modificarePentru combaterea durerii se poate interveni:
- Împiedicarea formării influxului nervos, în terminațiile senzitive: anestezice locale, miorelaxante, vasodilatatoare, antiinflamatoare.
2. Împiedicarea transmiterii influxului nervos, prin fibrele senzitive - cazul anestezicelor locale.
3. Împiedicarea perceperii durerii, la nivelul centrilor de integrare: anestezice generale, analgezice antipiretice, analgezice morfinomimetice.
Farmacoterapie
modificareDurerile acute:
- Analgezice plus adjuvanti (AINS, antispastice, transchilizante).
2. Analgezice neopioide + adjuvanți - dureri slabe sau moderate.
3. Opioide slabe tip codeină + neopioide + adjuvanți - dureri persistente.
4. Opioide forte - dureri intense.
Durerile postoperatorii: - opioide: morfină, tramadol, codeină, pentazocină (Fortral) - neopioide: paracetamol (injectabil intravenos - Perfalgan), metamizol (Algocalmin)
Nevralgiile medicație fiziopatologică (carbamazepina se folosește pentru nevralgia de trigemen). Migrena: în cazul crizei se pot folosi: aspirină + metoclopramid, ergotamina, dihidroergotamina, sumatriptan. Analgezicele N 02 sunt împărțite în: N 02 A -Opioide, N 02 B -Analgezice și antipiretice, N 03 C -Antimigrenoase.[2]
Controlul endogen al durerii
modificareNocicepția este corelată cu mecanisme activate de stimuli care amenință integritatea organismului. La nivel periferic, fibrele tip C nemielinizate (nociceptori polimodali) sau fibrele mielinizate subțiri tip Adelta sunt excitate de stimuli noxici, direct sau indirect, prin procesele inflamatorii. Fibrele aferente nociceptive se termină în lamelele superficiale ale cornului dorsal medular unde informația este integrată și controlată. Aceste prime sinapse sunt modulate de către aminoacizii excitatori (Glutamat și Aspartat) și câteva peptide (substanța P, CGRP, colecistokinina, opioide endogene). Majoritatea căilor ascendente implicate în nocicepție sunt localizate în cadranul ventrolateral controlateral al măduvei (tracturile spinoreticular și spinotalamic). Mai multe situri supra-pinale sunt activate după stimularea nociceptivă: formațiunea reticulată a trunchiului cerebral (inclusiv subnucleus reticularis dorsalis), regiunea ponto-mezencefalică și talamusul. Amigdala și zone hipotalamice sunt implicate în reacțiile emoționale și adaptările neuro-endocrine la evenimentele noxice. Și cortexul (cingular, insular și somato-senzitiv) primește informații nociceptive. Semnalele nociceptive sunt modulate la toate nivelele de transmisie, cea mai studiată fiind modularea la nivel spinal. Semnalele spinale pot fi inhibate și prin activarea unor căi inhibitorii bulbospinale și eliberare de serotonină, noradrenalină și, indirect, opioide endogene.[3] Aferența nociceptivă înspre SNC nu este doar o recepție pasivă ci este subiectul modulării prin plasticitatea medulară și prin influența descendentă de la siturile supraspinale activate de o varietate de semnale din mediu, inclusiv semnalul nociceptiv însuși (acut sau persistent) și stimuli emoționali. Rolul semnificativ al receptorilor NMDA și al producției de NO în sensibilizarea centrală, în hiperalgezie și în durerea cronică a fost demonstrat în numeroase modele de injurie periferică. S-a dovedit că aferențele nociceptive sunt subiectul unei modulări descendente atât facilitatorie cât și inhibitorie de la sit-uri supra-spinale, bulbare. Modularea descendentă de la bulbul rostral ventro-medial pare să contribuie la hiperalgezia observată în țesuturile inflamate, la distanță de locul insultei (hiperalgezie secundară) și implică mecanisme similare celor din măduva spinării (receptori NMDA, producere de NO). Organismul răspunde la cererile crescânde fizice sau psihologice prin activarea axelor hipofizo-corticoadrenală și simpato-meduloadrenală. Hormonii produși prin aceste activări contribuie la răspunsul adaptativ al organismului în menținerea homeostaziei. Acțiunile lor includ creșterea consumului de energie, adaptarea sistemului cardio-vascular, recrutarea sistemului imun dar și învățarea și autoanalgezia. În acest sens suprimarea durerii poate fi văzută ca un răspuns adaptativ la stres. Este de notorietate că o mare proporție dintre victimele unei traume acute nu resimt nici o durere în perioada imediat următoare injuriei. Beecher raportează că 70% dintre soldații americani răniți în bătălia de la Anzio nu resimțeau nici o durere sau aceasta era atât de mică încât nu doreau nici o medicație analgetică Datele au fost confirmate de Melzack și col., care au găsit că aproximativ 1/3 din 138 de victime consecutive ale unor accidente prezentate la camera de gardă au avut o perioadă fără durere, chiar după injurii severe. Toate acestea indică că situațiile extraordinare pot declanșa puternice mecanisme endogene, localizate în sistemul nervos central, care, odată activate, sunt capabile să modifice profund reacția la stimulii dureroși ca și trăirea lor. Stresul este un determinant puternic pentru eliberarea opioidelor endogene. De exemplu beta-endorfina este foarte concentrată în hipofiză, iar stresul produce coeliberarea de opioide și ACTH din hipofiză. În plus medulo-suprarenala conține peptide opioide care sunt eliberate în aceleași circumstanțe care duc la eliberarea de catecolamine (noradrenalina și adrenalina, agoniști naturali de alfa2-receptori) la nivelul terminațiilor nervoase și a medulo-suprarenalei.
Legături externe
modificare- Durerea Arhivat în , la Wayback Machine.. Actualități în Neurologie
- Durerea poate fi o boală, nu doar un simptom, 13 iunie 2011, Marius Comper, Descoperă
- Mai rele decât NAȘTEREA sau EXTRACȚIA de MĂSEA. Vezi TREI BOLI care te fac să TE URCI pe pereți de DURERE, 22 septembrie 2012, Andreea Ciulac, Evenimentul zilei
Note
modificare- ^ Human Phenotype Ontology release 2018-03-08, accesat în
- ^ Rezumat_Teza_de_doctorat_Ciotu_Ionut_Cosmin.pdf
- ^ „Neurofiziologia durerii - Viața Medicală”. www.viata-medicala.ro. Accesat în .
Bibliografie
modificare- Constantin Arseni, Ion Oprescu, Ion, Durerea. București : Editura Didactică și Pedagogică, 1970, 204 p.
- Constantin Arseni, Ion Oprescu, Durerea : fiziopatologie clinică și terapeutică ,București : Editura Academiei Republicii Socialiste România, 1967
- Gheorghe Badiu, Durerea, prieten sau dușman?, București : Editura Medicală, 1986
- Abordarea terapeutică multidisciplinară a durerii Conf. Univ. Dr. Mariana FLORIA, medic rezident cardiologie Ioana CEOMÎRTAN-NEGRII, 2020
- Managementul durerii. Ghid practic sub redacția Ostin C. Mungiu Irina M. JABA, Editura „Gr. T. Popa” Iași, 2009
Lectură suplimentară
modificare- Babeș, Alexandru. Durerea. Istoria conviețuirii cu un vechi dușman. București, Editura Humanitas, 2023, 256 p. ISBN 978-973-50-7880-5
