Alotropia oxigenului
Dioxigenul, oxigenul molecular sau oxigenul gazos (în general denumit simplu oxigen) este o moleculă diatomică compusă din doi atomi de oxigen. Este un gaz (în condiții normale de temperatură și presiune) incolor, inodor și insipid. Există o altă varietate alotropică ale oxigenului, formată din trei atomi: O3, denumit ozon.
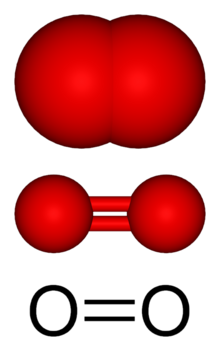
Alotropul cel mai comun al oxigenului elemental se numește dioxigen O
2, și are o lungime a legăturii de 121 pm și o energie de legătură de 498 kJ·mol−1.[1] Aceasta este forma care este utilizată de forme de viață complexe, cum ar fi animalele, în respirația celulară (vezi și rolul biologic) și este forma care are o mare importanță în atmosfera Pământului (vezi răspândire).[2]
În atmosfera terestră înaltă la peste 180 km este prezent oxigenul atomic.
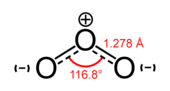
Trioxigenul (O
3) este cunoscut de obicei sub denumirea de ozon și este un alotrop al oxigenului foarte reactiv, dăunător pentru țesutul pulmonar.[3] Ozonul este produs în atmosfera superioară când O
2 se combină cu oxigenul atomic format prin diviziunea O
2 din cauza radiațiilor ultraviolete (UV).[4] Din moment ce ozonul este un puternic absorbant în regiunea ultravioletă a spectrului electromagnetic, stratul de ozon al atmosferei superioare funcționează ca un scut protector pentru radiațiile care sunt primite de planetă.[4] Totuși, în apropiere de suprafața terestră, este un poluant puternic, format ca produs secundar al gazelor de eșapament.[3] Molecula metastabilă de tetraoxigen (O
4) fost descoperită în 2001,[5][6] și se presupunea că ar exista în una dintre cele șase faze ale oxigenului solid. S-a demonstrat în anul 2006 că această fază, creată prin presurizarea dioxigenului la 20 GPa, este de fapt un cluster O
8 aparținând sistemului de cristalizare trigonal.[7] Acest cluster are un potențial de agent oxidant mult mai mare decât O
2 sau O
3, și prin urmare ar putea fi utilizat ca și combustibil pentru rachete.[5][6] În 1990 a fost descoperită o fază metalică a oxigenului solid, când acesta a fost supus unei presiuni mai mari de 96 GPa[8] și în 1998 s-a demonstrat că în condiții de temperatură foarte scăzută, devine un superconductor.[9]
Note
modificare- ^ Chieh, Chung. „Bond Lengths and Energies”. University of Waterloo. Arhivat din original la . Accesat în .
- ^ „Cellular Respiration”. IUPUI Department of Biology. Arhivat din original la . Accesat în .
- ^ a b Stwertka, Albert (). Guide to the Elements (ed. Revised). Oxford University Press. pp. 48–49. ISBN 0-19-508083-1.
- ^ a b Parks, G. D.; Mellor, J. W. (1939). Mellor's Modern Inorganic Chemistry (6th ed.). London: Longmans, Green and Co.
- ^ a b Cacace, Fulvio; de Petris, Giulia; Troiani, Anna (). „Experimental Detection of Tetraoxygen”. Angewandte Chemie International Edition. 40 (21): 4062–65. doi:10.1002/1521-3773(20011105)40:21<4062::AID-ANIE4062>3.0.CO;2-X. PMID 12404493.
- ^ a b Ball, Phillip (). „New form of oxygen found”. Nature News. Accesat în .
- ^ Lundegaard, Lars F.; Weck, Gunnar; McMahon, Malcolm I.; Desgreniers, Serge; Loubeyre, Paul (). „Observation of an O
8 molecular lattice in the phase of solid oxygen”. Nature. 443 (7108): 201–04. Bibcode:2006Natur.443..201L. doi:10.1038/nature05174. PMID 16971946. - ^ Desgreniers, S; =Vohra, Y. K.; Ruoff, A. L. (). „Optical response of very high density solid oxygen to 132 GPa”. J. Phys. Chem. 94 (3): 1117–22. doi:10.1021/j100366a020.
- ^ Shimizu, K.; =Suhara,, K.; Ikumo, M.; Eremets, M. I.; Amaya, K. (). „Superconductivity in oxygen”. Nature. 393 (6687): 767–69. Bibcode:1998Natur.393..767S. doi:10.1038/31656.