Limfocitul T citotoxic
O celulă T citotoxică (cunoscută și sub numele de T C, limfocit T citotoxic, CTL, celulă T ucigașă, celulă T citolitică, celule T CD8 + sau celulă T ucigașă) este un limfocit T (un tip de globulă albă) care distruge atât celule canceroase, cât și celule care sunt infectate cu agenți patogeni intracelulari (cum ar fi de exemplu virușii sau bacteriile) sau celulele care sunt deteriorate prin alte modalități.[1]
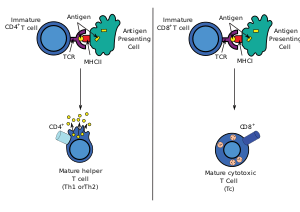
Majoritatea celulelor T citotoxice exprimă suprafața lorreceptori pentru celule T (TCR) care pot recunoaște un antigen specific. Un antigen este o moleculă capabilă să stimuleze un răspuns imun care este adesea indus de celulele canceroase, viruși, bacterii sau semnale intracelulare. Antigenul din interiorul unei celule este legat de molecule MHC de clasa I și prezentat la suprafața celulei de molecula MHC de clasa I, unde poate fi recunoscut de celula T. Dacă TCR este specific pentru acel antigen, acesta reacționează prin interacțiune directă cu complexul format din molecula MHC de clasa I și antigen, iar celula T distruge eventual celula.
Pentru ca TCR-ul să se lege specific de molecula MHC de clasa I, TCR-ul trebuie să fie însoțit de o glicoproteină supranumită CD8, care se leagă la rândul ei de porțiunea constantă a moleculei MHC de clasa I. Așadar, aceste celule T sunt numite celule T CD8 +.
Afinitatea care se stabilește între CD8 și molecula MHC menține conexiunea directă dintre celula T C și celula țintă în timpul activării specifice antigenului. Celulele T CD8 + sunt recunoscute ca fiind celule T C odată ce sunt activate. Celulele T CD8+ sunt în general clasificate ca având un rol citotoxic predefinit și foarte eficient în sistemul imunitar. Cu toate acestea, celulele T CD8 + au, de asemenea, capacitatea de a produce citokine (de exemplu TNF-α și IFN-γ) cu efecte antitumorale și antimicrobiene.
Dezvoltare
modificareSistemul imunitar trebuie să fie capabil să recunoască milioane de potențiali antigeni, pentru a se putea apăra. Însă există mai puține gene decât antigeni. În corpul uman există mai puțin de 30.000 de gene, așa că este imposibil să existe o genă pentru fiecare antigen în parte. Cu toate acestea, ADN-ul din milioane de globule albe din măduva osoasă este amestecat și reorganizat pentru a crea celule cu receptori unici, fiecare având capacitatea de a se lega de un antigen diferit. Unii receptori se leagă de țesuturile din corpul uman însuși, pentru a împiedica organismul să se atace pe sine, acele globule albe auto-reactive sunt distruse în timpul dezvoltării ulterioare în timus, locul unde iodul este necesar pentru dezvoltarea și activitatea sa.[2]
TCR-urile au două porțiuni: un lanț alfa și un lanț beta. (unii TCR au un lanț gamma și delta. Ele sunt specializate pentru a acționa împotriva stresului și fac parte din bariera epitelială[3]). Celulele stem hematopoietice din măduva osoasă migrează către timus, unde sunt supuse unei recombinări V(D)J a ADN-ului lanțului beta pentru a rezulta o versiune dezvoltată a proteinei TCR, cunoscută sub numele de pre-TCR. Dacă această rearanjare are loc cu succes, celulele își rearanjează ADN-ul lanțului alfa pentru a crea un complex TCR alfa-beta funcțional. Acest produs de rearanjare genetică foarte flexibilă în genele TCR-ului ajută la crearea a milioane de celule T diferite care exprimă TCR diferiți, ajutând sistemul imunitar al organismului să răspundă la aproape orice proteină a unui invadator sau a unui agent patogen. Majoritatea celulelor T exprimă TCR alfa-beta (celule T αβ), dar unele celule T din țesuturile epiteliale (de exemplu intestinul) exprimă TCR gamma-delta (celule T gamma delta), care recunosc antigene non-proteice. TCR gamma-delta se caracterizează prin capacitatea de a recunoaște antigenele care nu sunt prezentate pe suprafața celulară a agentului patogen. În plus, TCR menționați anterior pot recunoaște proteinele de șoc toxic microbiene și proteinele de stres auto-celular.[4] Celulele T γδ posedă o flexibilitate funcțională largă după recunoașterea celulelor infectate sau transformate. Acest lucru se datorează faptului că sunt capabile să producă citokine (ca de exemplu: IFN-γ, TNF-α, IL-17) și chemokine (ca de exemplu: IP-10, limfotactina), declanșând citoliza celulelor țintă, (perforine, granzime...) și interacționează cu alte celule, cum ar fi celulele epiteliale, monocitele sau celulele dendritice, cât și neutrofilele și celulele B. În unele infecții, cum ar fi citomegalovirusul uman, există o expansiune clonală a celulelor T γδ periferice care au TCR-uri specifice, indicând natura adaptativă a răspunsului imun mediat de aceste celule.[5]
Celulele T care prezintă un TCR stabil din punct de vedere funcțional exprimă atât co-receptorii CD4 cât și CD8. Astfel, aceste celule T sunt redenumite celule T „dublu pozitive” (DP) (CD4 + CD8 +). Celulele T dublu pozitive sunt expuse la o mare varietate de auto-antigene în timus și sunt ulterior supuse a două criterii de selecție strictă:
- selecție pozitivă, în care acele celule T dublu pozitive care se leagă la antigenul străin în prezența auto-MHC. Celulele T se vor diferenția fie în CD4 +, fie în CD8 +, în funcție de care MHC este asociat cu antigenul prezentat (MHC1 pentru CD8, MHC2 pentru CD4). În acest caz, celulele ar fi venit în contact cu antigenul în contextul MHC1. Selecția pozitivă înseamnă selectarea acelor TCR capabile să recunoască moleculele MHC self.
- selecție negativă, în care acele celule T dublu-pozitive care se leagă prea puternic de auto-antigenele prezentate de MHC suferă apoptoză, deoarece altfel ar putea deveni autoreactive, ceea ce duce la autoimunitate.
Celulele T care se leagă cu o afinitate scăzută la complexele MHC-auto-antigen sunt selectate pozitiv. Celulele care trec de selecția pozitivă și negativă se diferențiază în celule T de tip unic pozitiv, care fie prezintă pe suprafața lor CD4 sau CD8, în funcție de dacă TCR-ul lor recunoaște un antigen MHC de clasă I (CD8) sau un antigen MHC de clasa II (CD4).). Celulele T CD8 + sunt cele care se vor maturiza și vor deveni celule T citotoxice după activarea lor cu un antigen restricționat de clasa I.
Activare[necesită clarificare]
modificareCelulele T trec prin diferite etape de diferențiere și maturare, în funcție de frecvența cu care intract în contact cu un antigen specific. Inițial, limfocitele T naive sunt acelea care nu au întâlnit încă niciun antigen în timus. Ulterior, limfocitele T naive pot deveni celule T cu memorie. Acest tip de celule T sunt cele care au fost în contact cu un antigen specific cel puțin o dată. Insă, ulterior s-au reîntors la o stare inactivă, latentă. Cu toate acestea, ele sunt gata să răspundă din nou la antigenul împotriva căruia au fost stimulate. În cele din urmă, atunci când răspunsul imun specific este declanșat, aceste celule T naive și de memorie sunt activate, dând naștere la celule T efectoare care au capacitatea de a ucide agenții patogeni sau celulele tumorale.[6][7]
Pragul de activare al acestor celule este foarte mare, iar procesul de activare poate avea loc prin două modalități diferite: o cale timus-independentă (dirijată de către APC-uri infectate) sau una timus dependentă (dirijată de această data de către celulele T CD4+). În calea timus-independentă, deoarece APC-ul este infectat, este puternic activat și exprimă un număr mare de co-receptori pentru coactivare. Dacă APC-urile nu sunt infectate, celulele CD4 trebuie să fie implicate: fie pentru a activa APC prin co-stimulare (mai frecventă), fie pentru a activa direct celula Tc prin secretarea IL-2.
Dacă are loc activarea, limfocitul T își polarizează granulele spre locul sinapsei dintre el însuși și celula targhetată. Limfocitul T eliberează granulele, producând o „lovitură letală”. În acest moment, se separă de celula țintă și poate trece la alta și alta. Celula țintă moare în aproximativ 6 ore, de obicei prin apoptoză.[8]
MHC de clasa I este exprimat de către toate celulele gazdă pe suprafața lor. Excepție de la această regulă fac celule nenucleate (de exemplu, eritrocitele). Când aceste celule sunt infectate cu un agent patogen intracelular, celulele degradează proteinele străine prin procesarea antigenului. Acestea au ca rezultat fragmente de peptide, dintre care unele sunt prezentate de către MHC Clasa I receptorului de antigen al celulei T (TCR) pe celulele T CD8 +.
Activarea celulelor T CD8+ citotoxice este dependentă de o incursiune de interacțiuni simultane între moleculele exprimate pe suprafața celulei T (TCR, dar nu numai) și moleculele de pe suprafața celulei prezentatoare de antigen (APC). Drept exemplu se poate lua în considerare modelul cu două semnale pentru activarea celulelor T C.
| Semnal | celula T | APC | Descriere |
| Primul Semnal | TCR | moleculă MHC clasa I legată de peptidă | Există o a doua interacțiune între coreceptorul CD8 și molecula MHC de clasa I pentru a stabiliza acest semnal. |
| Al doilea semnal | moleculă CD28 de pe celula T | fie CD80, fie CD86 (numiți și B7-1 și B7-2) | CD80 și CD86 sunt cunoscuți ca costimulatori pentru activarea celulelor T. Acest al doilea semnal poate fi asistat (sau înlocuit) prin stimularea celulei T C cu citokine eliberate de celulele T helper. |
Activarea celulelor T CD8 + naive necesită interacțiunea cu un tip de celule profesionale capabile de prezentatoare de antigen, drept exemplu standard fiind celulele dendritice maturate. Pentru a se dezvolta în celule T cu memorie de lungă durată și pentru a permite stimularea ulterioară a celulelor T CD8+ citotoxice, celulele dendritice maturate trebuie să interacționeze nu doar cu celulele T CD4 + active, cât și cu celulele T CD8 + citotoxice.[7][9] În timpul acestui proces, celulele T helper CD4 + „autorizează” celulele dendritice pentru a oferi un semnal puternic de activare celulelor T CD8 + naive.[10]
În plus, maturarea celulelor T CD8 + citotoxice este mediată de semnalizarea CD40 -dependentă.[11] În momentul în care celula T CD8 + naivă este legată de celula infectată, celula infectată va elibera CD40.[11] Această eliberare de CD40, cu ajutorul celulelor T helper CD4+, va declanșa diferențierea celulelor T CD8 + naive la celulele T CD8 + mature.[11]
Activarea este dependentă de recunoașterea antigenului TCR. Însă, au fost descrise căi alternative de activare. De exemplu, celulele T citotoxice s-au dovedit a fi activate atunci când sunt vizate de alte celule T CD8, ducând la tolerarea acestora din urmă.[12]
O celulă T C activată suferă o proliferare clonală (dintr-o singură celulă va rezulta o expansiune semnificativă) cu ajutorul citokinei interleukinei 2 (IL-2), care este un factor de creștere și diferențiere pentru celulele T. Acest lucru crește numărul de celule specifice pentru antigenul țintă care pot călători apoi în tot corpul în căutarea celulelor somatice pozitive pentru antigen.
Funcții efectoare
modificareCând sunt expuse la celule somatice infectate și/sau disfuncționale, celulele T C activate eliberează citotoxine precum perforina, granzimele și granulizina. Prin acțiunea perforinei, granzimele traversează membrana celulei țintă și pătrund în citoplasma acesteia. Funcția granzimelor de serin proteaze declanșează așa numita cascadă a caspazelor, care este o serie de cistein proteaze care duc în cele din urmă la apoptoză (moartea celulară programată). Aceasta se numește „lovitură letală” și permite observarea unei morți sub formă de val a celulelor țintă.[13] Datorită ordinului ridicat al lipidelor și fosfatidilserinei încărcate negativ prezente în membrana lor plasmatică, celulele T C sunt rezistente la efectele perforinei și citotoxinelor lor granzime.[14]
Un al doilea mecanism prin care se poate induce apoptoza este prin interacțiunea directă dintre suprafața celulară a TC și a celulei patogene, sau în general a celulei țintă. Când un TC este activat, acesta exprimă extracelular ligandul FAS al proteinei de suprafață (FasL)(Apo1L)(CD95L). FasL se poate lega specific la moleculele Fas (Apo1)(CD95) exprimate extracelular de celula țintă. Însă, în ciuda celor menționate, această interacțiune dintre cele două componente Fas-Fas este considerată a fi mai degrabă vitală pentru eliminarea limfocitelor T nedorite/nefavorabile în timpul dezvoltării lor sau pentru activitatea litică a anumitor celule T H CD4+, în detrimentul activității citolitice a celulelor efectoare T C. Interacțiunea dintre Fas și FasL permite recrutarea ulterioară a complexului de semnalizare indusă de moarte (DISC).[15] Domeniul letal asociat cu Fas (FADD) se translocă cu DISC, permițând recrutarea procaspazelor 8 și 10.[15] Aceste caspaze activează apoi caspazele efectoare 3, 6 și 7, ducând la scindarea substraturilor morții, cum ar fi lamina A, lamina B1, lamina B2, PARP (poli ADP riboză polimerază) și ADN-PKcs (protein kinaza activată de ADN). Rezultatul final este apoptoza celulei care a exprimat Fas. Celulele T CD8 pot prezenta, de asemenea, moartea celulară indusă de activare sau AICD, care este mediată de complexul receptorului CD3. Recent, s-a demonstrat că o proteină TLT-1 eliberată de trombocite induce moartea celulară asemănătoare AICD în celulele T CD8[16]
Se speculează că factorul de transcripție Eomesodermin joacă un rol extrem de important în funcția celulelor T CD8 +citotoxice. Acest factor acționează drept o genă reglatoare în răspunsul imun adaptativ.[17] Studiile care cercetează efectul unui deficit al funcției Eomesodermin au descoperit că o scădere a expresiei acestui factor de transcripție a dus la scăderea cantității de perforină produsă de celulele T CD8 +.[17]
Rolul în patogeneza bolii
modificareAnticorpii sunt eficienți atât împotriva infecțiilor virale, cât și a celor bacteriene. Însă, celulele T citotoxice sunt în mare parte eficiente împotriva virușilor.[18]
Atunci când gazda este infectată cu virusul hepatitei B (VHB), celulele T citotoxice ucid celulele infectate. Totodată, ele produc citokine antivirale capabile să elimine VHB din hepatocite. Cu toate acestea, celulele T citotoxice joacă, de asemenea, un rol patogen extrem de important. Acesta se datorează contribuției lor la aproape toate leziunile hepatice asociate cu infecția cu VHB.[19] S-a demonstrat că trombocitele facilitează acumularea de celule T citotoxice specifice virusului în ficatul infectat.[20] În unele studii pe șoareci, injectarea cu celule T CXCR5+ CD8+ arată o scădere semnificativă a HBsAg. De asemenea, o creștere a nivelurilor de CXCL13 a facilitat recrutarea celulelor intrahepatice CXCR5+CD8+T și, aceste tipuri de celule au produs niveluri ridicate de interferon specific HBV (IFN)-γ și IL-21, care pot ajuta la îmbunătățirea controlului asupra infecției cronice cu VHB.[21]
S-a descoperit că celulele T citotoxice au fost implicate în progresia artritei. Atunci când ne referim la poliartritei reumatoide este de menționat implicarea sa articulară. Membrana sinovială este caracterizată prin hiperplazie, vascularizare crescută și un infiltrat de celule inflamatorii, în principal limfocite T CD4+ ajutoare. Limfocitele ajutoare dirijează în principal răspunsurile imune mediate la nivel celular.Diferitele studii și cercetări în domeniu demonstrază că artrita reumatoidă este strâns corelată cu antigenele MHC-ului de clasa II. În acest context, este demn de menționat că singurele celule din organism care exprimă antigene MHC de clasă II sunt celulele constitutive prezentatoare de antigen. Acest lucru sugerează cu tărie că artrita reumatoidă este cauzată de antigene artritogenice neidentificate. Antigenul poate fi orice antigen exogen, ca de exemplu proteinele virale, sau o proteină endogenă.[22] Recent, au fost identificate un număr de posibile antigene endogene, cum ar fi de exemplu glicoproteina 39 a cartilajului uman, proteina de legare a lanțului greu și proteina citrulinată. Limfocitele T CD4+ ajutoare active stimulează monocitele, macrofagele și fibroblastele sinoviale pentru a elabora citokine (interleukina-1, interleukina-6 și factorul de necroză tumorală alfa (TNFa)) și pentru a secreta metaloproteinaze. Primele trei citokine menționate anterior sunt cheie în declanșarea inflamației în artrita reumatoidă. Aceste limfocite activate stimulează, de asemenea, celulele B să producă imunoglobuline, inclusiv factorul reumatoid.[23] Rolul lor patogen este necunoscut, dar se poate datora activării complementului prin formarea complexului imun. Mai mult, numeroase studii pe animale sugerează că celulele T citotoxice pot avea un efect predominant proinflamator în boală. De asemenea, se cercetează activ faptul că producția de citokine de către celulele CD8+ poate accelera progresul bolii artritei.[24]
S-a descoperit că celulele T CD8 + citotoxice joacă un rol important în infecția cu virusul HIV. Virusul HIV a dezvoltat de-a lungul timpului o varietate de strategii prin intermediul cărora acesta poate evada cu ușurință acțiunea sistemul imunitar al celulei gazdă. De exemplu, HIV a adoptat rate foarte mari de mutație pentru a permite virusului să scape de recunoașterea de către celulele T CD8 +.[25] Virusul este, de asemenea, capabil să regleze în mod negativ expresia proteinelor MHC de suprafață de clasa I a celulelor pe care le infectează, pentru a evita în continuare distrugerea de către celulele T CD8 +.[25] Dacă celulele T CD8 + nu pot găsi, recunoaște și lega de celulele infectate, virusul nu va fi distrus și va continua să crească.
În plus, celulele T CD8 + citotoxice pot avea un rol esențial în diabetul de tip 1.[26] Studiile preclinice realizate cu ajutorul unui model de șoarece diabetic au arătat că celulele CD4+ ajutoare sunt responsabile pentru infiltrarea masivă a leucocitelor mononucleare în insulele pancreatice. Cu toate acestea, s-a demonstrat că celulele CD8+ citotoxice joacă un rol efector. Acestea sunt responsabile pentru distrugerea finală a celulelor beta insulare. Însă, studiile pe șoareci NOD au demonstrat contrariul. Șoarecii NOD poartă o mutație nulă în locusul beta 2-microglobulinei (beta 2-mu) și deci au o deficiență de molecule majore de clasă I de histocompatibilitate și celule T CD8+. S-a constatat că aceștia totuși nu au dezvoltat diabet.[27]
- Citotoxicitate mediată de CTL
- celule T CD4 +
Note
modificare- ^ „Lymphocytes”. Advanced Hematology in Integrated Cardiovascular Chinese Medicine. Elsevier. . pp. 41–46. doi:10.1016/b978-0-12-817572-9.00007-0. ISBN 978-0-12-817572-9.
Helper T cells/CD4+ •express CD4 glycoproteins on their cell surface, which activate in the presence of peptide antigens on the surface of invading pathogens; •respond immediately to protect the immune system; •secrete different cytokine proteins according to the immune response.
- ^ „Iodine, thymus, and immunity”. Nutrition. 25 (9): 977–979. septembrie 2009. doi:10.1016/j.nut.2009.06.002. PMID 19647627.
- ^ „Features and functions of gamma delta T lymphocytes: focus on chemokines and their receptors”. Critical Reviews in Immunology. 23 (5–6): 339–370. . doi:10.1615/CritRevImmunol.v23.i56.10. PMID 15030305.
- ^ „Ligand recognition by the γδ TCR and discrimination between homeostasis and stress conditions”. Cellular & Molecular Immunology. 17 (9): 914–924. septembrie 2020. doi:10.1038/s41423-020-0503-y. PMC 7608190 . PMID 32709926.
- ^ „Characterization of Adaptive-like γδ T Cells in Ugandan Infants during Primary Cytomegalovirus Infection”. Viruses. 13 (10): 1987. octombrie 2021. doi:10.3390/v13101987. PMID 34696417.
- ^ Inmunología (de memoria) (ed. Cuarta edición). Ciudad de México: Médica Panamericana. . ISBN 978-968-7988-28-3. OCLC 1022564980.
- ^ a b „Concurrent interaction of DCs with CD4(+) and CD8(+) T cells improves secondary CTL expansion: It takes three to tango”. European Journal of Immunology. 44 (12): 3543–3559. decembrie 2014. doi:10.1002/eji.201444477. PMID 25211552.
- ^ Cellular and molecular immunology (ed. Ninth). Philadelphia, PA. . ISBN 978-0-323-52323-3. OCLC 973917896.
- ^ „Crosstalk between T lymphocytes and dendritic cells”. Critical Reviews in Immunology. 32 (2): 139–155. . doi:10.1615/CritRevImmunol.v32.i2.30. PMID 23216612.
- ^ „Immunology. Licence to kill”. Nature. 393 (6684): 413–414. iunie 1998. Bibcode:1998Natur.393..413L. doi:10.1038/30845. PMID 9623994.
- ^ a b c „Help for cytotoxic-T-cell responses is mediated by CD40 signalling”. Nature (în engleză). 393 (6684): 478–480. iunie 1998. Bibcode:1998Natur.393..478B. doi:10.1038/30996. PMID 9624004.
- ^ „CTLs respond with activation and granule secretion when serving as targets for T-cell recognition”. Blood. 117 (3): 1042–1052. ianuarie 2011. doi:10.1182/blood-2010-05-283770. PMC 3035066 . PMID 21045195.
- ^ „Preparing the lethal hit: interplay between exo- and endocytic pathways in cytotoxic T lymphocytes”. Cellular and Molecular Life Sciences. 74 (3): 399–408. februarie 2017. doi:10.1007/s00018-016-2350-7. PMC 5241346 . PMID 27585956.
- ^ „Lipid order and charge protect killer T cells from accidental death”. Nature Communications. 10 (1): 5396. noiembrie 2019. Bibcode:2019NatCo..10.5396R. doi:10.1038/s41467-019-13385-x. PMC 6881447 . PMID 31776337.
- ^ a b „Cytotoxic T Lymphocytes”. Encyclopedia of Medical Immunology. . pp. 332–342. doi:10.1007/978-0-387-84828-0_36. ISBN 978-0-387-84827-3.
- ^ Tyagi, Tarun; et al. „Platelet-derived TLT-1 promotes tumor progression by suppressing CD8+ T cells”. doi:10.1084/jem.20212218.
- ^ a b „Control of effector CD8+ T cell function by the transcription factor Eomesodermin”. Science. 302 (5647): 1041–1043. noiembrie 2003. Bibcode:2003Sci...302.1041P. doi:10.1126/science.1090148. PMID 14605368.
- ^ „Type B coxsackieviruses and their interactions with the innate and adaptive immune systems”. Future Microbiology. 5 (9): 1329–1347. septembrie 2010. doi:10.2217/fmb.10.101. PMC 3045535 . PMID 20860480.
- ^ „Pathogenetic and antiviral immune responses against hepatitis B virus”. Future Virology. 1 (2): 189–96. . doi:10.2217/17460794.1.2.189.
- ^ „Platelets mediate cytotoxic T lymphocyte-induced liver damage”. Nature Medicine. 11 (11): 1167–1169. noiembrie 2005. doi:10.1038/nm1317. PMC 2908083 . PMID 16258538.
- ^ „CXCL13-mediated recruitment of intrahepatic CXCR5+CD8+ T cells favors viral control in chronic HBV infection”. Journal of Hepatology. 72 (3): 420–430. martie 2020. doi:10.1016/j.jhep.2019.09.031. PMID 31610223.
- ^ „Antibody-dependent and -independent mechanisms of inflammatory arthritis”. JCI Insight. 4 (5): e125278. martie 2019. doi:10.1172/jci.insight.125278. PMID 30843881.
- ^ „The central role of T cells in rheumatoid arthritis”. Clinical and Experimental Rheumatology. 25 (5 Suppl 46): S4–11. septembrie 2007. PMID 17977483.
- ^ „Potential roles for CD8(+) T cells in rheumatoid arthritis”. Autoimmunity Reviews. 12 (3): 401–409. ianuarie 2013. doi:10.1016/j.autrev.2012.07.011. PMID 22841983.
- ^ a b „CD8+ T-cells: function and response to HIV infection”. Current HIV Research. 2 (1): 23–37. ianuarie 2004. doi:10.2174/1570162043485077. PMID 15053338.
- ^ „CD8+ T cells in type 1 diabetes”. Advances in Immunology. 100: 79–124. . doi:10.1016/S0065-2776(08)00804-3. PMID 19111164.
- ^ „The role of CD8+ T cells in the initiation of insulin-dependent diabetes mellitus”. European Journal of Immunology. 26 (8): 1762–1769. august 1996. doi:10.1002/eji.1830260815. PMID 8765018.
Legături externe
modificare- Materiale media legate de Limfocit T citotoxic la Wikimedia Commons
- T-cell Group - Cardiff University