Reacție SN2
Reacția SN2, cu denumirea completă de reacție de substituție nucleofilă bimoleculară, este un tip de reacție de substituție nucleofilă, în care etapa determinantă de viteză este bimoleculară (două specii moleculare sunt implicate în etapa lentă).[1][2]
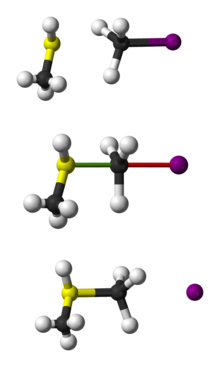
Mecanism
modificareReacția are loc adesea la un carbon alifatic hibridizat sp3, care are atașat un atom electronegativ (de obicei notat X), de obicei un atom de halogen. Ruperea legăturii C-X și formarea noii legături (notată C-Y sau C-Nu) are loc concomitent, simultan, sau prin intermediul unei stări de tranziție, în care avem un atom de carbon pentacoordinat. Atacul nucleofil are loc din direcția inversă nucleofugului (X), iar acesta părăsește molecula în partea opusă, având loc inversia geometriei tetraedrice de la atomul central de carbon.
Dacă substratul conține un centru chiral, atunci prin atacul nucleofil are loc o inversie a configurației moleculare, numită inversie Walden.
Un exemplu este reacția SN2 dintre Br− (nucleofilul) și clorura de etil (electrofilul), din care rezultă bromoetanul. Nucleofugul este anionul clorură:
Stereochimie
modificareCompetiția cu eliminarea
modificareEfectul solventului
modificareVezi și
modificareReferințe
modificare- ^ L. G. Wade, Jr., Organic Chemistry, 6th ed., Pearson/Prentice Hall, Upper Saddle River, New Jersey, USA, 2005
- ^ McMurry, John E. Organic Chemistry (1992), (3rd ed.), Belmont: Wadsworth, ISBN 0-534-16218-5