Tiocianat de amoniu
| Tiocianat de amoniu | |
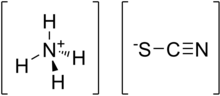 | |
| Nume IUPAC | Tiocianat de amoniu |
|---|---|
| Alte denumiri | Sulfocianat/sulfocianură de amoniu |
| Identificare | |
| ChEMBL | CHEMBL3187560 |
| PubChem CID | 13417437 15666, 13417437 |
| Informații generale | |
| Formulă chimică | NH4SCN |
| Aspect | cristale higroscopice incolore |
| Masă molară | 76,122 g/mol |
| Proprietăți | |
| Densitate | 1,305 g/cm3 |
| Punct de topire | 149,5 °C |
| Punct de fierbere | 170 °C |
| Solubilitate în apă | |
| 128 g/100 mL (0 °C) | |
| Pericol | |
| Fraze R | R32, R20/21/22, R52/53 |
| Fraze S | S13, S61 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Tiocianatul de amoniu este un compus anorganic cu formula NH4SCN, sarea cationului amoniu cu acidul tiocianic.
Obținere
modificareTiocianatul de amoniu poate fi obținut în urma reacției dintre sulfură de carbon și amoniac în soluția apoasă, în condiții de temperatură și presiune ridicate (se formează ca și intermediar ditiocarbamatul de amoniu):
Proprietăți chimice
modificareTiocianatul de amoniu este stabil în prezența aerului, dar prin încălzire se transformă în tiouree:
Ca și tiocianatul de potasiu, tiocianatul de amoniu este folosit în analiza chimică pentru identificarea cationului trivalent de fier Fe3+. Astfel, o soluție apoasă de tiocianat adăugată la soluția unei săruri de fier trivalent (sare ferică, cum este clorura ferică) va forma o soluție de colorație roșu-sângerie, specifică tiocianatului de fier (III):[1]
Reacționează cu hidroxidul de potasiu cu formarea de tiocianat de potasiu și hidroxid de amoniu:
Referințe
modificare- ^ Raluca Ripan, Ervin Popper, Candin Liteanu (1961), Chimie analitică calitativă, București, Editura de Stat Didactică și Pedagogică; p. 158
- A. F. Wells, Structural Inorganic Chemistry, 5th ed., Oxford University Press, Oxford, UK, 1984. ISBN 978-0198553700


