Defect cardiac congenital
| Acest articol (sau secțiunea de mai jos) conține greșeli de ortografie sau de punctuație. Puteți consulta manualul de stil și contribui prin corectarea greșelilor. |
| Defect cardiac congenital | |
 | |
| Specialitate | cardiologie |
|---|---|
| Clasificare și resurse externe | |
| ICD-11 | |
| ICD-9-CM | 746.9[1] |
| OMIM | 234750 |
| DiseasesDB | 17017 |
| MedlinePlus | 001114 |
| MeSH ID | D006330[2][1] |
| Modifică date / text | |
Defectul cardiac congenital ( DCC ), cunoscut și sub denumirea de anomalie cardiacă congenitală și boală cardiacă congenitală, este un defect în structura inimii sau a vaselor mari care este prezent încă de la naștere . [3] Semnele și simptomele depind de tipul specific de defect. Simptomele pot varia de la lipsă până la cel care poate pune viața în pericol. Când sunt prezente, simptomele pot include respirație rapidă, piele albăstruie (cianoză), creștere lentă în greutate și senzație de oboseală. Defectele cardiace congenitale nu provoacă dureri în piept. [4] Majoritatea defectelor cardiace congenitale nu sunt asociate cu alte boli. [5] O complicație a defectului cardiac congenital este insuficiența cardiacă .
Cauza unui defect cardiac congenital este adesea necunoscută. [6] Factorii de risc includ anumite infecții în timpul sarcinii, cum ar fi rubeola, utilizarea anumitor medicamente, alcoolul sau tutunul, moștenirea genetică de la părinții sau starea nutrițională slabă sau obezitatea mamei. [5] [7] A avea un părinte cu un defect cardiac congenital este, de asemenea, un factor de risc. [8] O serie de afecțiuni genetice sunt asociate cu defecte cardiace, inclusiv sindromul Down, sindromul Turner și sindromul Marfan . Defectele cardiace congenitale sunt împărțite în două grupe principale: defecte cardiace cianotice și defecte cardiace non-cianotice, în funcție de predispoziția pielii copilului de a deveni albăstruie. Defectele pot implica pereții interiori ai inimii, valvele inimii sau vasele mari de sânge care duc spre și dinspre inimă. [3]
Defectele cardiace congenitale pot fi prevenite parțial prin vaccinarea antirubeolă, prin adăugarea de iod în sare și prin adăugarea de acid folic la anumite produse alimentare. [5] Unele defecte nu au nevoie de tratament. [3] Altele pot fi tratate eficient cu proceduri pe bază de cateter sau chirurgie cardiacă . Ocazional poate fi nevoie de un număr de operații, [9] sau un transplant de inimă . Cu un tratament adecvat, rezultatele sunt în general bune, chiar și cu probleme complexe.
Defectele cardiace congenitale sunt cele mai frecvente defecte la naștere . [5] [10] În 2015, au fost prezenți la 48,9 milioane de oameni la nivel global. [11] Acestea afectează între 4 și 75 de indivizi la 1000 de nașteri vii, în funcție de modul în care sunt diagnosticate. [8] În aproximativ 6 până la 19 cazuri la 1000 de nașteri vii, acestea cauzează un grad de probleme moderat până la sever. Defectele cardiace congenitale sunt principala cauză a deceselor cauzate de defecte la naștere: în 2015, acestea au dus la 303.300 de decese, în scădere față de 366.000 de decese în 1990. [12] [13]
Semne și simptome
modificareSemnele și simptomele sunt legate de tipul și severitatea defectului cardiac. Simptomele sunt prezente frecvent la începutul vieții, dar este posibil ca unele DCC să nu fie detectate de-a lungul vieții. [14] Unii copii nu au semne, în timp ce alții pot prezenta respirație, cianoză, leșin, [15] murmur cardiac, subdezvoltare a membrelor și mușchilor, alimentație sau creștere deficitară sau infecții respiratorii. Defectele cardiace congenitale provoacă o structură anormală a inimii, ceea ce duce la producerea anumitor sunete numite murmur cardiac . Acestea pot fi uneori detectate prin auscultare ; cu toate acestea, nu toate murmururile inimii sunt cauzate de defecte cardiace congenitale.
Condiții asociate
modificareDefectele cardiace congenitale sunt asociate cu o incidență crescută a altor șapte afecțiuni medicale specifice, fiind numite împreună asociația VACTERL :
- V - anomalii vertebrale
- A - atrezie anală
- C - anomalii cardiovasculare
- T - fistula traheoesofagiană
- E - atrezie esofagiană
- R - anomalii renale și / sau radiale
- L - defecte ale membrelor
Defectul septal ventricular (DSV), defectele septale atriale și tetralogia Fallot sunt cele mai frecvente defecte cardiace congenitale observate în asociația VACTERL. Defecțiuni mai puțin frecvente în asociere sunt truncus arteriosus și transpunerea marilor artere.
Cauze
modificareCauza bolilor congenitale de inimă poate fi genetică, de mediu sau o combinație a ambelor. [16]
Genetică
modificareMutațiile genetice, adesea sporadice, reprezintă cea mai mare cauză cunoscută a defectelor cardiace congenitale. [17] Acestea sunt descrise în tabelul de mai jos.
| Leziuni genetice | Procent procentabil | Exemple | Metoda de testare genetică primară |
|---|---|---|---|
| aneuploidies | 5-8% [16] | Trisomii autosomale supraviețuitoare (cromozomi 13, 18, 21 ), monosomia X cromozomului (sindrom Turner) | karyotyping |
| Copiați variantele de număr | 10-12% [18] | Ștergere / dublare 22q11.2 (sindromul velocardiofacial / DiGeorge), 1 ștergere / duplicare q21.1, ștergere / duplicare 8p23.1, ștergere 15q11.2 (sindromul Burnside-Butler) | Hibridizare comparativă genomică Array (cunoscută și sub numele de analiză cromosomică microarray) |
| Variantă cu un singur nucleotid (SNV) care codifică proteine moștenite sau inserție / ștergere mică (indel) | 3-5% [19] | Sindromul Holt-Oram, sindrom Noonan, sindrom Alagille | Panou de gene |
| SNV de codificare a proteinelor De novo sau indel | ~ 10% [20] [17] | Mutațiile genelor foarte exprimate în timpul dezvoltării inimii | Secvențiere între exome |
Căi moleculare
modificareGenele care reglementează secvența complexă de dezvoltare au fost elucidate doar parțial. Unele gene sunt asociate cu defecte specifice. O serie de gene au fost asociate cu manifestările cardiace. Mutațiile unei proteine musculare cardiace, lanțul greu de α-miozină ( MYH6 ) sunt asociate cu defecte septale atriale. Mai multe proteine care interacționează cu MYH6 sunt, de asemenea, asociate cu defecte cardiace. Factorul de transcriere GATA4 formează un complex cu Tbx5 care interacționează cu MYH6. Un alt factor, gena homeobox (de dezvoltare), NKX2-5 interacționează, de asemenea, cu MYH6. Mutațiile tuturor acestor proteine sunt asociate atât cu defecte septice atriale, cât și ventriculare; În plus, NKX2-5 este asociat cu defecte în conducta electrică a inimii și TBX5 este legat de sindromul Holt-Oram care include defecte de conducere electrică și anomalii ale membrului superior. O altă genă T-box, TBX1, este implicată în sindromul velo-cardio-facial al sindromului DiGeorge, cea mai frecventă ștergere care are simptome extinse, inclusiv defecte ale tractului de ieșire cardiac, inclusiv tetralogia Fallot . [21]
| MYH6 | GATA4 | Nkx2-5 | Tbx5 | TBX1 | |
|---|---|---|---|---|---|
| loc | 14q11.2-q13 | 8p23.1-p22 | 5q34 | 12q24.1 | 22q11.2 |
| Sindromul | Holt-Oram | DiGeorge | |||
| Defecte septale atriale | ✔ | ✔ | ✔ | ✔ | |
| Defecte septale ventriculare | ✔ | ✔ | ✔ | ||
| Anomalii de conducere electrică | ✔ | ✔ | |||
| Anomalii ale tractului de ieșire | ✔ | ||||
| Manifestări non-cardiace [22] | Anomalii ale membrelor superioare | Mici sau absente timus </br> Paratiroizi mici sau absenți </br> Anomalii faciale |
Calea de semnalizare Noch, un mecanism de reglementare pentru creșterea și diferențierea celulelor, joacă un rol larg în mai multe aspecte ale dezvoltării cardiace. Elementele de creștere sunt implicate în determinarea laturilor drepte și stângi ale planului corpului, astfel încât plierea direcțională a tubului cardiac poate fi afectată. Semnalizarea de creștere este implicată în formarea pernelor endocardice și continuă să fie activă pe măsură ce se dezvoltă în septe și valve. Este, de asemenea, implicat în dezvoltarea peretelui ventricular și conectarea tractului de ieșire la marile vase. Mutațiile genei pentru unul dintre liganzii de crestătură, Jagged1, sunt identificate în majoritatea cazurilor examinate de displazie arteriohepatică ( sindromul Alagille ), caracterizată prin defecte ale marilor vase (stenoză arterială pulmonară), inimă ( tetralogie a Fallot în 13% cazuri), ficat, ochi, față și oase. Deși mai puțin de 1% din toate cazurile, în care nu se găsesc defecte în gena Jagged1, se găsesc defecte în gena Notch2 . În 10% din cazuri, nu există nicio mutație în niciuna dintre gene. Pentru un alt membru al familiei de gene, mutațiile din gena Notch1 sunt asociate cu valva aortică bicuspidă, o supapă cu două pliante în loc de trei. Notch1 este, de asemenea, asociat cu calcifierea valvei aortice, a treia cea mai frecventă cauză a bolilor de inimă la adulți. [23] [24]
Mutațiile unui mecanism de reglare a celulelor, calea Ras / MAPK sunt responsabile pentru o varietate de sindroame, inclusiv sindromul Noonan, sindromul LEOPARD, sindrom Costello și sindromul cardiofaciocutanat în care există o implicare cardiacă. [25] În timp ce condițiile enumerate sunt cunoscute cauze genetice, există multe alte gene care sunt mai subtile. Se știe că riscul de defecte cardiace congenitale este mai mare atunci când există o rudă apropiată cu unul. [26]
De mediu
modificareFactorii cunoscuți de mediu includ anumite infecții în timpul sarcinii, cum ar fi rubeola, medicamente ( alcool, hidantoină, litiu și talidomidă ) și boli materne ( diabet zaharat, fenilcetonurie și lupus eritematos sistemic ). [27]
Fiind supraponderal sau obez crește riscul de boli cardiace congenitale. [7] În plus, pe măsură ce obezitatea maternă crește, crește și riscul de defecte cardiace. [28] Nu a fost identificat un mecanism fiziologic distinct care să explice legătura dintre obezitatea maternă și CHD, dar atât deficiența de folat pre-sarcină, cât și diabetul au fost implicate în unele studii. [29]
Mecanism
modificareExistă o secvență complexă de evenimente care au ca rezultat o inimă bine formată la naștere și perturbarea oricărei porțiuni poate duce la un defect. [26] Momentul ordonat al creșterii celulare, al migrației celulare și al morții celulare programate („ apoptoza ”) a fost studiat pe larg și sunt elucidate genele care controlează procesul. [21] În jurul zilei de dezvoltare 15, celulele care vor deveni inima există în două benzi în formă de potcoavă ale stratului de țesut mediu ( mezoderm ), și unele celule migrează dintr-o porțiune a stratului exterior ( ectoderm ), creasta neurală, care este sursa unei varietăți de celule găsite în tot corpul. În ziua 19 de dezvoltare, se formează o pereche de elemente vasculare, „tuburile endocardice”. Tuburile fuzionează atunci când celulele suferă de moarte programată, iar celulele din primul câmp al inimii migrează spre tub și formează un inel de celule cardiace ( miocite ) în jurul lui până în ziua 21. În ziua 22, inima începe să bată și până în ziua 24, sângele circulă. [30]
În ziua 22, sistemul circulator este bilateral simetric, cu vasele împerecheate pe fiecare parte și inima constând dintr-un tub simplu situat în linia mediană a dispunerii corpului. Porțiunile care vor deveni atria și vor fi situate cel mai aproape de cap sunt cele mai îndepărtate de cap. În zilele 23 până la 28, tubul cardiac se pliază și se răsucește, viitoarele ventricule deplasându-se la stânga din centru (locația finală a inimii) și atriile se mișcă spre cap. [30]
În ziua 28, zonele de țesut din tubul inimii încep să se extindă spre interior; după aproximativ două săptămâni, aceste extinderi, „ septul primum ” membranos și „ pernele endocardice ” musculare, fuzionează pentru a forma cele patru camere ale inimii. Nerespectarea corectă a fuziunii va duce la un defect care poate permite scurgerea sângelui între camere. După ce se întâmplă, celulele care au migrat de pe creasta neurală încep să împartă cordusul bulbus, traiectul principal de ieșire este împărțit în două prin creșterea unui sept spiralat, devenind marile vase - segmentul ascendent al aortei și al trunchiului pulmonar. Dacă separarea este incompletă, rezultatul este o „arterioză truncus persistentă”. Vasele pot fi inversate („ transpunerea marilor vase ”). Cele două jumătăți ale tractului divizat trebuie să migreze în pozițiile corecte peste ventriculele corespunzătoare. O defecțiune poate duce la curgerea unor sânge în vasul greșit (de exemplu, aortă suprasolicitată ). Inima cu patru camere și marile vase au trăsături necesare pentru creșterea fătului. Plămânii sunt neexpandiți și nu pot găzdui volumul circulator complet. Două structuri există pentru a evita fluxul de sânge departe de plămâni. Celulele dintr-o parte a septului primum mor creând o gaură în timp ce celulele musculare, „ septum secundum ”, cresc de-a lungul părții atriale drepte septum primum, cu excepția unei regiuni, lăsând un gol prin care sângele poate trece de la artiumul drept la atriul stâng, foramen ovale . Un vas mic, ductus arteriosus permite ca sângele din artera pulmonară să treacă în aortă. [30]
Modificări la naștere
modificareDuctus arteriosus rămâne deschis din cauza factorilor de circulație, inclusiv prostaglandinele . Foramenul ovale rămâne deschis din cauza fluxului de sânge din atriul drept spre atriul stâng. Pe măsură ce plămânii se extind, sângele curge ușor prin plămâni și porțiunea membranoasă a foramenului ovale (septul primum) se plutește peste porțiunea musculară (septum secundum). Dacă închiderea este incompletă, rezultatul este un brevet foramen ovale . Cele două clapete pot fuziona, dar mulți adulți au un foramen ovale care rămâne închis doar din cauza diferenței de presiune dintre atrii. [30]
Teorii
modificareRokitansky (1875) a explicat defectele cardiace congenitale ca rupturi în dezvoltarea inimii în diferite etape ale ontogenezei . [31] Spitzer (1923) le tratează ca revenind la una din etapele filogenezei . [32] Krimsky (1963), sintetizând două puncte de vedere anterioare, a considerat bolile cardiace congenitale ca o oprire a dezvoltării la un anumit stadiu al ontogenezei, corespunzând cu aceasta sau acea etapă a filogenezei. [33] Prin urmare, aceste teorii pot explica doar tipuri de defecte feminine și neutre.
Diagnostic
modificareMulte defecte cardiace congenitale pot fi diagnosticate prenatal prin ecocardiografie fetală . Acesta este un test care se poate face în al doilea trimestru de sarcină, când femeia are aproximativ 18-24 săptămâni de sarcină. [34] Poate fi o ecografie abdominală sau o ecografie transvaginală .
Dacă un copil se naște cu boli cardiace cianotice, diagnosticul se face de obicei la scurt timp după naștere, datorită culorii albastre a pielii sale (numită cianoză). [34]
Dacă un copil se naște cu un defect septal sau un defect de obstrucție, de multe ori simptomele lor se observă numai după câteva luni sau uneori chiar și după mulți ani. [34]
Clasificare
modificareO serie de sisteme de clasificare există pentru defecte cardiace congenitale. În 2000, a fost dezvoltată Nomenclatura internațională a chirurgiei cardiace congenitale pentru a furniza un sistem de clasificare generică. [35]
Hipoplazie
modificareHipoplazia poate afecta inima, rezultând de obicei subdezvoltarea ventriculului drept sau a ventriculului stâng . Acest lucru face ca o singură parte a inimii să fie capabilă să pompeze sângele în corp și în plămâni în mod eficient. Hipoplazia inimii este rară, dar este cea mai gravă formă de CHD. Se numește sindrom hipoplastic cardiac stâng atunci când afectează partea stângă a inimii și hipoplastic sindromul cardiac drept atunci când afectează partea dreaptă a inimii. În ambele condiții, prezența unui brevet ductus arteriosus (și, atunci când hipoplazia afectează partea dreaptă a inimii, un foramen ovale patentat ) este vitală pentru capacitatea sugarului de a supraviețui până când se poate efectua operația de urgență cardiacă, deoarece fără aceste căi de sânge nu poate circula către corp (sau plămâni, în funcție de ce parte a inimii este defectă). Hipoplazia inimii este în general un defect cardiac cianotic . [36]
Defecte obstructive
modificareDefectele obstructive apar atunci când valvele cardiace, arterele sau venele sunt anormal înguste sau blocate . Defectele obișnuite includ stenoza pulmonară, stenoza aortică și coarctarea aortei, cu alte tipuri precum stenoza a valvei aortice bicuspide și stenoza subaortică fiind relativ rare. Orice îngustare sau blocaj poate cauza mărirea inimii sau hipertensiune arterială . [37]
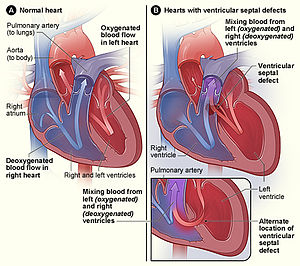
Defecte septale
modificareSeptul este un perete de țesut care separă inima stângă de cea dreaptă . Defectele din septul interatrial sau septul interventricular permit sângelui să curgă din partea dreaptă a inimii spre stânga, reducând eficiența inimii. [37] Defectele septale ventriculare sunt colectiv cel mai frecvent tip de CHD, [38] deși aproximativ 30% dintre adulți au un tip de defect septal atrial numit patent sond foramen ovale . [39]
Defecte cianotice
modificareDefectele cardiace cianotice sunt numite astfel, deoarece acestea au ca rezultat cianoza, o decolorare a cenușii-albăstrui a pielii din cauza lipsei de oxigen în organism. Astfel de defecte includ truncus arteriosus persistent, conexiunea venoasă pulmonară anomală totală, tetralogia Fallot, transpunerea marilor vase și atresia tricuspidă . [37]
Defecte
modificare- Stenoza aortica
- Defect septal atrial (ASD)
- Defect septal atrioventricular (AVSD)
- Valva aortică bicuspidă
- cardiomiopatia
- Bloc cardiac complet (CHB)
- dextrocardia
- Ventriculul stâng dublu de intrare (DILV)
- Ventriculul drept dublu de ieșire (DORV)
- Anomalia lui Ebstein
- Sindromul hipoplazic al inimii stângi (HLHS)
- Sindromul hipoplazic al inimii drepte (HRHS)
- Stenoza mitrala
- Truncus arteriosus persistent
- Atrezie pulmonară
- Stenoza pulmonară
- Rabdomioame (Tumori ale inimii)
- Transpunerea marilor vase
- dextro-Transpunerea marilor artere (d-TGA)
- levo-Transpunerea marilor artere (l-TGA)
- Atresie tricuspidă
- Defect septal ventricular (VSD)
- Sindromul Wolff-Parkinson-White (WPW)
Unele afecțiuni afectează marile vase sau alte vase aflate în imediata apropiere a inimii, dar nu și inima însăși, dar sunt adesea clasificate drept defecte cardiace congenitale.
- Coarctarea aortei (CoA)
- Arcul dublu aortic, artera subclaviană aberantă și alte malformații ale marilor artere
- Arcul aortic întrerupt (IAA)
- Brevet ductus arteriosus (PDA)
- Sindromul Scimitar (SS)
- Conexiune venoasă pulmonară anomală parțială (PAPVC)
- Conexiune venoasă pulmonară anomală totală (TAPVC)
Unele constelații ale mai multor defecte sunt frecvent întâlnite împreună.
- Tetralogia Fallot (ToF)
- Pentalogia lui Cantrell
- Sindromul Shone / complexul lui Shone / anomalia Shone
Tratament
modificareCHD poate necesita o intervenție chirurgicală și medicamente. Medicamentele includ diuretice, care ajută organismul în eliminarea apei, sărurilor și digoxinei pentru întărirea contracției inimii. Acest lucru încetinește bătăile inimii și elimină puțin lichid din țesuturi. Unele defecte necesită proceduri chirurgicale pentru a readuce circulația înapoi la normal și, în unele cazuri, sunt necesare mai multe intervenții chirurgicale.
Cardiologia intervențională oferă pacienților alternative minim invazive la intervenția chirurgicală pentru unii pacienți. Valva pulmonară Melody Transcatheter (TPV), aprobată în Europa în 2006 și în SUA în 2010 în cadrul unei scutiri de dispozitive umanitare (HDE), este proiectată pentru a trata pacienții cu boli cardiace congenitale cu un conduct disfuncțional în tractul de ieșire ventriculară dreaptă (RVOT) . RVOT este conexiunea dintre inimă și plămâni; odată ce sângele ajunge în plămâni, este îmbogățit cu oxigen înainte de a fi pompat către restul corpului. Tehnologia valvei pulmonare Transcatheter oferă un mijloc mai puțin invaziv pentru a prelungi durata de viață a unei conducte RVOT eșuate și este proiectată pentru a permite medicilor să livreze o supapă pulmonară de înlocuire printr-un cateter prin vasele de sânge ale pacientului.
Multe persoane necesită îngrijire cardiacă specializată pe viață, mai întâi cu un cardiolog pediatru și mai târziu cu un cardiolog congenital pentru adulți. Există mai mult de 1,8 milioane de adulți care trăiesc cu defecte cardiace congenitale. [40]
Epidemiologie
modificareDefectele cardiace sunt printre cele mai frecvente defecte la naștere, care apar la 1% dintre nașteri vii (2-3% inclusiv valva aortică bicuspidă). [10] În 2013, 34,3 milioane de persoane aveau CHD. În 2010, acestea au avut ca rezultat 223.000 de decese, în scădere față de 278.000 de decese în 1990 [41]
Pentru defectele cardiace congenitale care apar fără antecedente familiale ( de novo ), riscul de recurență la urmași este de 3-5%. [42] Acest risc este mai mare în obstrucțiile tractului de ieșire ventricular stâng, heterotaxie și defecte septale atrioventriculare.
Terminologie
modificareDefectele cardiace congenitale sunt cunoscute printr-o serie de nume, inclusiv anomalia cardiacă congenitală, boli cardiace congenitale, defecte cardiace și malformații cardiovasculare congenitale. [43]
Vezi și
modificare- Societatea de chirurgi cardiaci congenitali
Referințe
modificare- ^ a b Disease Ontology, accesat în
- ^ Human Phenotype Ontology release 2018-03-08, accesat în
- ^ a b c „What Are Congenital Heart Defects?”. National Heart, Lung, and Blood Institute. . Arhivat din original la . Accesat în .
- ^ „What Are the Signs and Symptoms of Congenital Heart Defects?”. National Heart, Lung, and Blood Institute. . Arhivat din original la . Accesat în .
- ^ a b c d Shanthi Mendis; Pekka Puska; Bo Norrving; World Health Organization (). Global Atlas on Cardiovascular Disease Prevention and Control (PDF). World Health Organization in collaboration with the World Heart Federation and the World Stroke Organization. pp. 3, 60. ISBN 978-92-4-156437-3. Arhivat din original (PDF) la . Accesat în .
- ^ „What Causes Congenital Heart Defects?”. National, Heart, Lung, and Blood Institute. . Arhivat din original la . Accesat în .
- ^ a b „Preconception care: nutritional risks and interventions”. Reproductive Health. 11 Suppl 3: S3. septembrie 2014. doi:10.1186/1742-4755-11-s3-s3. PMC 4196560 . PMID 25415364.
- ^ a b Milunsky, Aubrey (). „1”. Genetic Disorders and the Fetus: Diagnosis, Prevention and Treatment. John Wiley & Sons. ISBN 9781444358216.
- ^ „How Are Congenital Heart Defects Treated?”. National Heart, Lung, and Blood Institute. . Arhivat din original la . Accesat în .
- ^ a b Vos, Theo; Barber, Ryan M.; Bell, Brad; Bertozzi-Villa, Amelia; Biryukov, Stan; Bolliger, Ian; Charlson, Fiona; Davis, Adrian; Degenhardt, Louisa (august 2015). „Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013”. Lancet. 386 (9995): 743–800. doi:10.1016/S0140-6736(15)60692-4. PMC 4561509 . PMID 26063472.
- ^ Vos, Theo; Allen, Christine; Arora, Megha; Barber, Ryan M.; Bhutta, Zulfiqar A.; Brown, Alexandria; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J. (octombrie 2016). „Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015”. Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577 . PMID 27733282.
- ^ Wang, Haidong; Naghavi, Mohsen; Allen, Christine; Barber, Ryan M.; Bhutta, Zulfiqar A.; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J.; Chen, Alan Zian (octombrie 2016). „Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015”. Lancet. 388 (10053): 1459–1544. doi:10.1016/s0140-6736(16)31012-1. PMC 5388903 . PMID 27733281.
- ^ GBD 2013 Mortality Causes of Death Collaborators (ianuarie 2015). „Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013”. Lancet. 385 (9963): 117–71. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604 . PMID 25530442.
- ^ „Heart Defects: Birth Defects”. Merck. Arhivat din original la . Accesat în .
- ^ „National Heart, Lung, and Blood Institute”. Arhivat din original la . Accesat în .
- ^ a b Hoffman, J. (). Essential Cardiology: Principles and Practice. Totowa, NJ: Humana Press. p. 393. ISBN 978-1-58829-370-1.
- ^ a b „Advances in the Genetics of Congenital Heart Disease: A Clinician's Guide”. Journal of the American College of Cardiology. 69 (7): 859–870. februarie 2017. doi:10.1016/j.jacc.2016.11.060. PMID 28209227.
- ^ „The importance of copy number variation in congenital heart disease”. NPJ Genomic Medicine. 1: 16031. septembrie 2016. doi:10.1038/npjgenmed.2016.31. PMC 5505728 . PMID 28706735.
- ^ „Changing Landscape of Congenital Heart Disease”. Circulation Research. 120 (6): 908–922. martie 2017. doi:10.1161/CIRCRESAHA.116.309302. PMID 28302739.
- ^ „Genetics and Genomics of Congenital Heart Disease”. Circulation Research. 120 (6): 923–940. martie 2017. doi:10.1161/CIRCRESAHA.116.309140. PMC 5557504 . PMID 28302740.
- ^ a b „Making or breaking the heart: from lineage determination to morphogenesis”. Cell. 126 (6): 1037–48. septembrie 2006. doi:10.1016/j.cell.2006.09.003. PMID 16990131.
- ^ Jones, Kenneth Lyons (). Smith's recognizable patterns of human malformation (ed. 5th). W.B. Saunders. pp. 316–317, 616–617. ISBN 978-0-7216-6115-5.
- ^ „Notch signaling in cardiac development”. Circulation Research. 102 (10): 1169–81. mai 2008. doi:10.1161/CIRCRESAHA.108.174318. PMID 18497317.
- ^ Spinner, N. B.; Leonard, L. D.; Krantz, I. D.; Adam, M. P.; Ardinger, H. H.; Pagon, R. A.; Wallace, S. E.; Bean LJH; Stephens, K. (). „Alagille Syndrome”. GeneReviews. PMID 20301450.
- ^ „The RASopathies: developmental syndromes of Ras/MAPK pathway dysregulation”. Current Opinion in Genetics & Development. 19 (3): 230–6. iunie 2009. doi:10.1016/j.gde.2009.04.001. PMC 2743116 . PMID 19467855.
- ^ a b Schoen, Frederick J.; Richard N., Mitchell (). „12. The Heart”. În Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson; Aster, Jon C. Robbins and Cotran Pathologic Basis of Disease (ed. 8th). Saunders Elsevier. ISBN 978-1-4160-3121-5.
- ^ „Factors Contributing to Congenital Heart Disease”. Lucile Packard Children’s Hospital at Stanford. Arhivat din original la . Accesat în .
- ^ „Maternal obesity and congenital heart defects: a population-based study”. The American Journal of Clinical Nutrition. 91 (6): 1543–9. iunie 2010. doi:10.3945/ajcn.2009.28865. PMC 2869507 . PMID 20375192.
- ^ „Prepregnancy obesity and birth defects: what's next?”. The American Journal of Clinical Nutrition. 91 (6): 1539–40. iunie 2010. doi:10.3945/ajcn.2010.29666. PMID 20427732.
- ^ a b c d Larsen, William J. (). „7. Development of the Heart”. Human Embryology. Churchill Livingstone. ISBN 978-0-443-08724-0.
- ^ Rokitarisky K. E. (1875) Die defecte der Scheidewande des Herzens. Wien.
- ^ Spitzer A. (1923) Arch. Pathol. Anat. 243, 81–272.
- ^ Krimski L. D. (1963) Pathological anatomy of congenital heart defects and complications after their surgical treatment. M., Medicine.
- ^ a b c „Archived copy”. Arhivat din original la . Accesat în .
- ^ Thomas P. Shanley; Derek S. Wheeler; Hector R. Wong (). Pediatric critical care medicine: basic science and clinical evidence. Berlin: Springer. p. 666. ISBN 978-1-84628-463-2.
- ^ „Hypoplastic Left Heart Syndrome”. American Heart. Arhivat din original la . Accesat în .
- ^ a b c „Congenital Cardiovascular Defects”. American Heart. Arhivat din original la . Accesat în .
- ^ „Ventricular Septal Defect”. eMedicine Health. Arhivat din original la . Accesat în .
- ^ „Circulatory Changes at Birth”. University of California at Berkeley. Arhivat din original la . Accesat în .
- ^ „Adult Congenital Heart Association”. Adult Congenital Heart Association. Arhivat din original la . Accesat în .
- ^ „Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010”. Lancet. 380 (9859): 2095–128. decembrie 2012. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
- ^ „Management of Pregnancy in Patients With Complex Congenital Heart Disease: A Scientific Statement for Healthcare Professionals From the American Heart Association”. Circulation. 135 (8): e50–e87. februarie 2017. doi:10.1161/CIR.0000000000000458. PMID 28082385.
- ^ „Other Names for Congenital Heart Defects”. . Arhivat din original la . Accesat în .
Legături externe
modificare- Defect cardiac congenital pe Curlie
- Informații despre boli cardiace congenitale Arhivat în , la Wayback Machine. pentru părinți.