Ciclohexan
| Ciclohexan | |
 | |
 | |
 | |
| Nume IUPAC | n-ciclohexan |
|---|---|
| Identificare | |
| Număr CAS | 110-82-7 |
| ChEMBL | CHEMBL15980 |
| PubChem CID | 8078 |
| Informații generale | |
| Formulă chimică | C6H12 |
| Aspect | lichid incolor |
| Masă molară | 84,16 g/mol |
| Proprietăți | |
| Densitate | 0,7781 g/mL |
| Starea de agregare | lichid |
| Punct de topire | 6,47 °C |
| Punct de fierbere | 80,74 °C |
| Solubilitate | imiscibil în apă; solubil în acetonă, alcool, eter; |
| Presiune de vapori | 78 mm Hg[1] |
| Indice de refracție(nD) | 1,42662 |
| Viscozitate | 1,02 cP la 17 °C |
| Pericol | |
| Fraze R | R11, R38, R65, R67, R50/53 |
| Fraze S | S9, S16, S33, S60, S61, S62 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
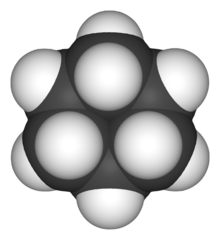
Ciclohexanul este un cicloalcan cu formula moleculară C6H12. Compusul este folosit ca solvent nepolar în industria chimică, și de asemenea ca materie primă pentru producerea industrială a acidului adipic și a caprolactamului, care sunt ambii compuși intermediari pentru fabricarea nailonului.
Producere și utilizare
modificareLa scară industrială, ciclohexanul se obține prin reacția dintre benzen și hidrogen. Producătorii de ciclohexan folosesc aproximativ 11,4% din cererea totală de benzen la nivel mondial. [2] Datorită proprietăților chimice și conformaționale unice, ciclohexanul este de asemenea utilizat în analiza chimică și ca standard. Are un miros aparte asemănător detergentului.
Geometrie
modificareRotația în jurul legăturilor C-C permite moleculei de ciclohexan să adopte o infinitate de conformații. Atunci când se reprezintă molecula de ciclohexan în 3 dimensiuni, pot exista în condiții normale două conformații: „scaun” și „baie”. (denumiri conform C.D.Nenițescu) Prima formă este mai stabilă decât cea de-a doua.
-
Conformaţia de tip scaun
-
Conformaţia de tip baie
-
Formulă topologică
Istoric
modificareîn 1894, Baeyer a sintetizat ciclohexanul pornind de la acidul pimelic, pe care l-a supus unei condensări Dieckmann, iar apoi a realizat reduceri multiple:
și în anelași an, E. Haworth și W.H. Perkin Jr. (1860–1929) au făcut același lucru plecând de la 1,6-dibromohexan și folosindu-se de reacția Wurtz.
Astăzi, ciclohexanul poate fi sintetizat cu ajutorul benzenului trecut prin diverse reacții de reducere. [3]
Vezi și
modificareNote
modificare- ^ http://www.cdc.gov/niosh/npg/npgd0163.html Lipsește sau este vid:
|title=(ajutor) - ^ en Market Study Benzene, Ceresana, iulie 2011 [1] Arhivat în , la Wayback Machine.
- ^ Fred Fan Zhang, Thomas van Rijnman, Ji Soo Kim, Allen Cheng. On Present Methods of Hydrogenation of Aromatic Compounds, 1945 to Present Day. Lunds Tekniska Högskola 2008
Bibliografie
modificare- C.D.Nenițescu Chimie Organică, vol. I, ediția a VII-a, Editura Didactică și Pedagogică, 1973, pag. 241-243 (cap. Ciclohexanul și derivații săi)




